Integração entre TRL, empreendedorismo e ética como base da inovação responsável em saúde.
Aldemar Araujo Castro
Criação: 21/01/2026
Atualização: 21/02/2026
Palavras: 1285
Tempo de leitura: 6 minutos
Resumo
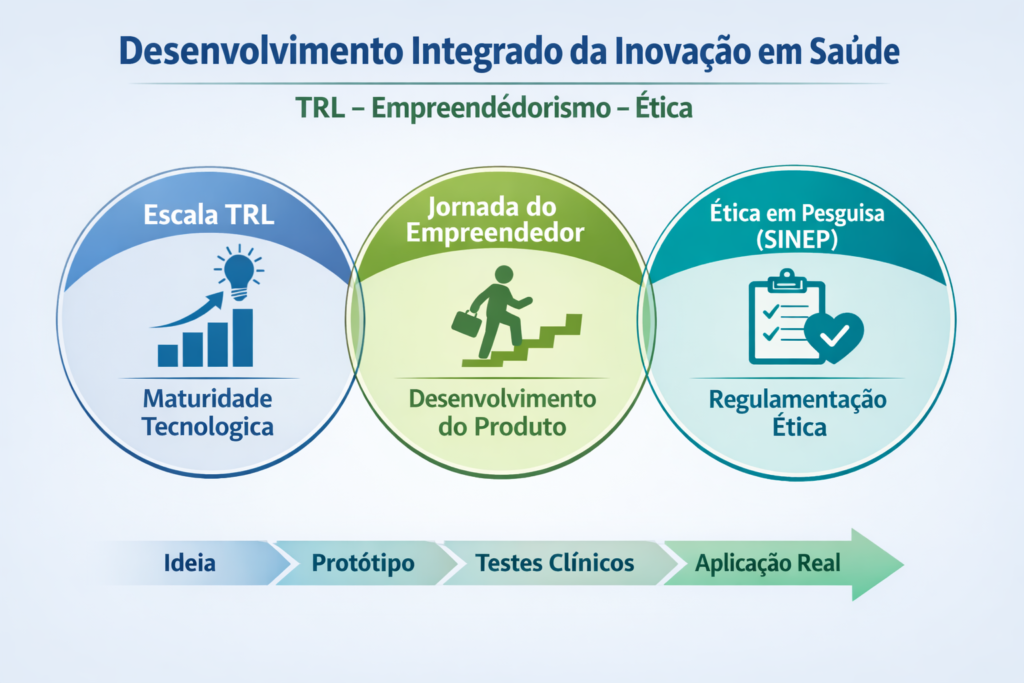
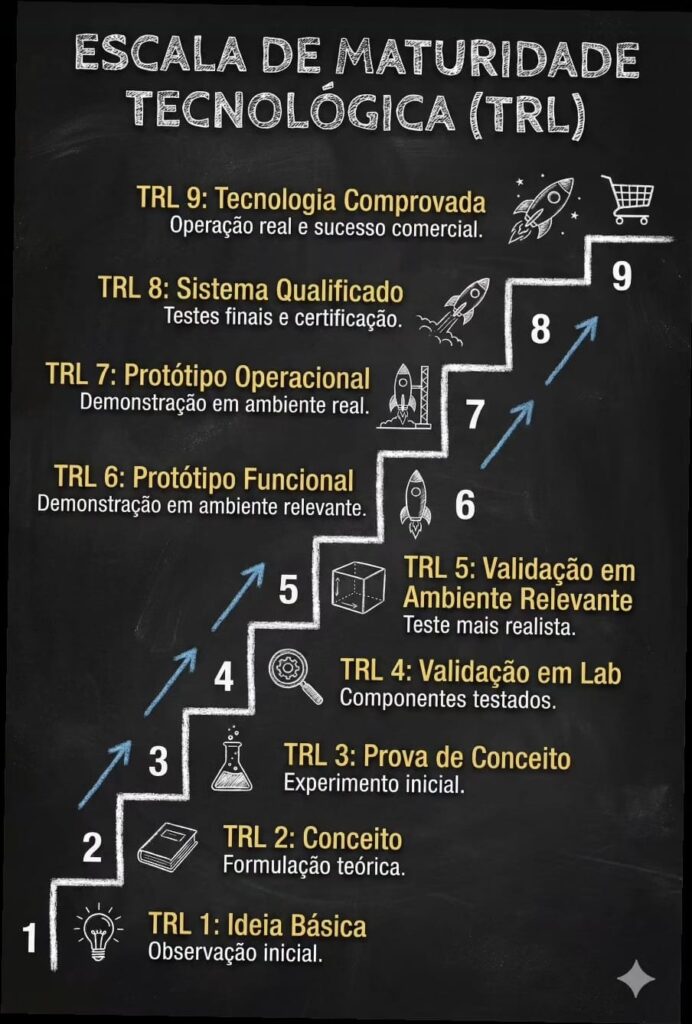
A inovação em saúde exige alinhamento entre maturidade tecnológica, desenvolvimento do produto e rigor ético. A Escala de Maturidade Tecnológica, TRL (Technology Readiness Level), avalia o grau de prontidão de uma tecnologia, enquanto a jornada do empreendedor descreve sua evolução como solução aplicável e sustentável. No Brasil, a ética em pesquisa com seres humanos é regulada pelo Sistema Nacional de Ética em Pesquisa, SINEP, que acompanha o aumento progressivo do risco ao longo desse percurso. Este capítulo propõe uma abordagem integrada desses três eixos, utilizando como exemplo o desenvolvimento de uma nova Bota de Unna para o tratamento de úlceras venosas. A articulação entre TRL, empreendedorismo e ética contribui para reduzir falhas metodológicas, evitar pendências éticas recorrentes e promover inovação tecnicamente sólida, clinicamente relevante e socialmente responsável.
Introdução
A inovação em saúde ocupa uma posição singular entre os processos de produção científica e tecnológica, pois seus resultados impactam diretamente a vida, a segurança e a dignidade das pessoas. Por essa razão, inovar em saúde não pode ser compreendido apenas como avanço técnico ou eficiência produtiva, mas como um percurso que exige método, responsabilidade e compromisso ético desde as fases iniciais até a consolidação da tecnologia no mundo real.
Apesar dessa complexidade, muitos projetos de pesquisa e inovação ainda são conduzidos de forma fragmentada. A maturidade tecnológica, o desenvolvimento do produto enquanto solução empreendedora e a avaliação ética progressiva costumam ser tratados como dimensões independentes, quando na realidade constituem eixos interdependentes de um mesmo processo. Essa dissociação explica parte significativa das pendências éticas recorrentes, dos atrasos regulatórios e das dificuldades de transposição do conhecimento científico para a prática clínica. A Escala de Maturidade Tecnológica (TRL, Technology Readiness Level), a jornada do empreendedor e o Sistema Nacional de Ética em Pesquisa (SINEP, antigo CEP/CONEP), quando analisados de forma integrada, oferecem um arcabouço robusto para superar essas fragilidades.
Desenvolvimento integrado da inovação em saúde sob os eixos TRL, empreendedorismo e ética
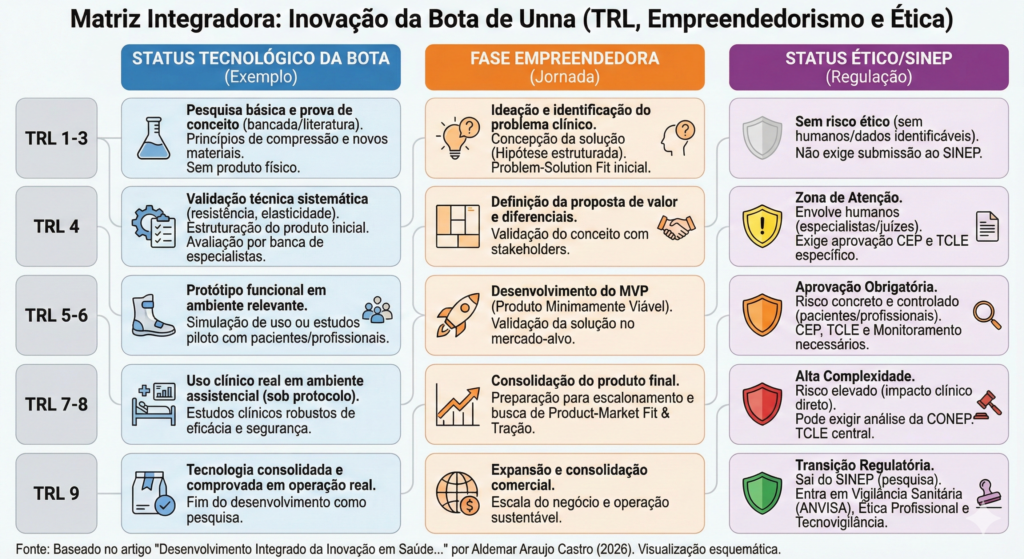
O desenvolvimento de uma nova Bota de Unna constitui um exemplo didático e tecnicamente relevante para demonstrar a interdependência entre maturidade tecnológica, amadurecimento empreendedor e exigências éticas progressivas. Embora seja um dispositivo terapêutico tradicional no manejo das úlceras venosas dos membros inferiores, qualquer inovação em sua formulação, estrutura ou modo de aplicação reabre todo o ciclo de validação científica, ética e regulatória. A aparente simplicidade do produto não reduz a complexidade do processo de inovação.
TRL 1 a 3, ideação tecnológica, concepção empreendedora e ausência de exigência ética
Nos níveis iniciais de maturidade tecnológica, o desenvolvimento da nova Bota de Unna situa se no domínio da pesquisa básica e da prova de conceito. Investiga-se princípios científicos relacionados à compressão terapêutica, às propriedades físico químicas de novos materiais e à plausibilidade de melhorias em relação ao modelo convencional. Os experimentos ocorrem em bancada e na consulta a literatura, sem aplicação clínica imediata.
Na jornada do empreendedor, essa fase corresponde à identificação aprofundada do problema clínico e à concepção inicial da solução. Ainda não existe produto, apenas hipótese estruturada.
Sob o ponto de vista ético, não há envolvimento de seres humanos nem uso de dados clínicos identificáveis. O risco ético é inexistente, não havendo exigência de submissão ao SINEP.
TRL 4, validação técnica inicial, estruturação do produto e zona de atenção ética
O avanço para o TRL 4 marca a transição da formulação conceitual para a validação técnica sistemática. Os componentes da nova Bota de Unna passam a ser avaliados quanto à resistência mecânica, elasticidade, durabilidade, estabilidade da formulação e capacidade de manter compressão terapêutica adequada.
Na jornada do empreendedor, esse estágio corresponde à estruturação do produto inicial. A solução começa a adquirir forma concreta, com definição mais clara de proposta de valor, diferenciais técnicos e viabilidade de aplicação.
Um elemento frequentemente incorporado nessa fase é a utilização de uma banca de juízes, composta por especialistas com experiência clínica e técnica no manejo de úlceras venosas. Esses especialistas avaliam de forma estruturada aspectos como aplicabilidade, coerência técnica, plausibilidade de uso e potencial impacto clínico da inovação.
Do ponto de vista ético, a participação de uma banca de juízes caracteriza envolvimento de seres humanos em pesquisa, ainda que sem risco clínico direto. Trata-se de coleta sistematizada de julgamentos técnicos e opiniões especializadas, o que exige submissão prévia ao SINEP, apreciação por Comitê de Ética em Pesquisa e elaboração de Termo de Consentimento Livre e Esclarecido específico para esses participantes.
Assim, o TRL 4 configura uma zona de atenção ética ampliada. Além do eventual uso de dados secundários, cuja exigência ética depende de sua origem e grau de anonimização, a inclusão de especialistas como participantes avaliadores torna obrigatória a aprovação ética no âmbito do SINEP.
TRL 5 e 6, protótipo funcional, produto minimamente viável e aprovação ética obrigatória
Nos níveis TRL 5 e 6, a nova Bota de Unna atinge o estágio de protótipo funcional e passa a ser avaliada em ambiente relevante, simulando condições reais de uso. Isso pode envolver aplicação por profissionais treinados ou estudos piloto com pacientes.
Na jornada do empreendedor, essa fase corresponde ao desenvolvimento do produto minimamente viável (MVP) e à validação da solução.
Nesse estágio, há envolvimento direto ou indireto de seres humanos e coleta de dados clínicos. O risco ético torna-se concreto, ainda que controlado. A submissão ao SINEP é obrigatória, com análise pelo Comitê de Ética em Pesquisa, elaboração de Termo de Consentimento Livre e Esclarecido e definição de estratégias de monitoramento dos participantes.
TRL 7 e 8, uso clínico real, consolidação do produto e avaliação ética de alta complexidade
No TRL 7, a nova Bota de Unna passa a ser utilizada em ambiente assistencial real, ainda sob protocolo de pesquisa. O impacto direto sobre o cuidado torna o risco ético elevado.
Na jornada do empreendedor, ocorre a consolidação do produto final e a preparação para escalonamento.
Do ponto de vista ético, trata-se de fase de alta complexidade, frequentemente exigindo apreciação em instância nacional no âmbito do SINEP, especialmente quando há inovação relevante ou potencial impacto clínico ampliado. O Termo de Consentimento assume papel central como instrumento de comunicação ética.
No TRL 8, estudos clínicos mais robustos consolidam evidências de segurança e eficácia.
TRL 9, consolidação da tecnologia, escala empreendedora e transição regulatória
No TRL 9, a tecnologia é considerada comprovada em operação real. O desenvolvimento enquanto pesquisa se encerra.
Na jornada do empreendedor, inicia-se a fase de expansão e consolidação.
Sob o aspecto ético, a tecnologia encerra seu ciclo no escopo do SINEP (ética em pesquisa) e realiza a transição para o escopo da ética médica/profissional e da vigilância pós-comercialização (tecnovigilância), regulada por normas sanitárias (ANVISA), conselhos de classe, legislação de responsabilidade civil e LGPD.
Considerações finais
A análise integrada do desenvolvimento de uma nova Bota de Unna demonstra que a inovação em saúde exige alinhamento rigoroso entre maturidade tecnológica, amadurecimento empreendedor e avaliação ética progressiva. O SINEP atua como eixo estruturante da proteção humana ao longo desse percurso, acompanhando o aumento do risco e garantindo legitimidade social à inovação.
Inovar em saúde sem método é arriscar pessoas. Inovar sem ética é comprometer a credibilidade da ciência. Inovar sem visão empreendedora é limitar o impacto. A verdadeira inovação ocorre quando tecnologia, propósito e responsabilidade caminham juntas.
Fontes comentadas
-
NASA, Technology Readiness Level
Documento de referência que define a escala TRL e seus critérios técnicos.
https://www.nasa.gov/directorates/heo/scan/engineering/technology/technology_readiness_level -
European Commission, Horizon Europe TRL guidance
Guia oficial que relaciona TRL a inovação e financiamento em pesquisa.
https://ec.europa.eu/info/funding-tenders/opportunities/docs/2021-2027/horizon/guidance/trl_en.pdf -
Conselho Nacional de Saúde, Resolução nº 466 de 2012
Marco normativo central da ética em pesquisa com seres humanos no Brasil.
https://conselho.saude.gov.br/resolucoes/2012/Reso466.pdf -
Conselho Nacional de Saúde, Carta Circular nº 1 de 2021 CONEP
Orientações sobre pesquisas com coleta de dados em ambiente virtual.
https://conselho.saude.gov.br/images/Oficios/2021/Carta_Circular_01_2021_CONEP.pdf -
OECD, Technology Readiness and Innovation Policy
Discussão conceitual sobre maturidade tecnológica e políticas de inovação.
https://www.oecd.org/innovation/inno/technology-readiness.htm
***