Guia prático sobre diretrizes de relato (checklists) para qualificar a pesquisa científica em saúde
Aldemar Araujo Castro
Criação: 09/01/2026
Atualização: 13/01/2026
Palavras: 1895
Tempo de leitura: 9 minutos
Resumo
A integridade e a utilidade da literatura médica dependem fundamentalmente da clareza e da precisão com que os estudos são relatados. A omissão de detalhes metodológicos cruciais impede a reprodução de pesquisas e a avaliação crítica de seus resultados. Este artigo compila e descreve as principais diretrizes de relato (reporting guidelines) recomendadas internacionalmente pela rede Equator Network. Apresentamos uma revisão prática das ferramentas essenciais para diferentes desenhos de estudo, incluindo o CONSORT para ensaios clínicos, STROBE para estudos observacionais, PRISMA para revisões sistemáticas, entre outros checklists especializados como SPIRIT e AGREE II. O objetivo é oferecer aos pesquisadores um roteiro para estruturar manuscritos que atendam aos mais altos padrões de transparência, reduzindo riscos de viés e aumentando as chances de aceitação em periódicos de alto impacto.
Palavras-chave: Redação Científica; Metodologia de Pesquisa; Diretrizes de Relato; Medicina Baseada em Evidências; Equator Network.
Introdução
A comunicação científica eficaz é o pilar fundamental da Medicina Baseada em Evidências. Para que um estudo possa influenciar a prática clínica ou fundamentar novas investigações, ele deve ser relatado com clareza, transparência e integridade suficientes para permitir sua replicação e a avaliação crítica de sua validade interna e externa. No entanto, a literatura biomédica tem historicamente sofrido com descrições incompletas e relatos seletivos de desfechos, o que compromete a utilidade dos dados publicados e desperdiça recursos valiosos de pesquisa.
Em resposta a esse desafio, grupos internacionais de especialistas desenvolveram as Reporting Guidelines. Estas ferramentas, geralmente apresentadas na forma de checklists, diagramas de fluxo e textos explicativos, especificam um conjunto mínimo de informações que devem constar em um manuscrito. Diferente de guias de conduta ética ou de estilo, as diretrizes de relato focam na arquitetura metodológica: elas garantem que o leitor saiba exatamente o que foi feito, como foi feito e o que foi encontrado.
Atualmente, a adesão a essas diretrizes não é apenas uma recomendação de boa prática, mas uma exigência editorial da maioria dos periódicos de alto impacto. O uso correto dessas ferramentas guia os autores durante a redação, auxilia os revisores durante a avaliação por pares e, em última análise, eleva a qualidade da ciência disponível para a sociedade. Este artigo serve como um guia prático para as principais diretrizes vigentes, facilitando sua seleção e aplicação no cotidiano do pesquisador.
3. A Rede Equator: O Ponto de Partida
Antes de detalhar as diretrizes específicas, é crucial conhecer a fonte primária onde todas elas residem. A Equator Network (Enhancing the QUAlity and Transparency Of health Research) é uma iniciativa internacional que visa melhorar a confiabilidade e o valor da literatura de pesquisa médica através da promoção de práticas de relato transparentes e precisas.
O site da Equator funciona como uma “biblioteca dinâmica” que indexa milhares de diretrizes, não se limitando apenas às mais famosas. Para o pesquisador, o portal oferece árvores de decisão e ferramentas de busca que auxiliam na identificação do checklist exato para um desenho de estudo específico, mesmo que este seja um subtipo raro ou híbrido.
Sempre que houver dúvida sobre qual diretriz utilizar, a consulta inicial deve ser feita neste portal.
URL Oficial
https://www.equator-network.org
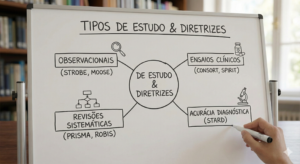
4. Diretrizes por Tipo de Estudo
Abaixo, categorizamos as diretrizes essenciais conforme o desenho metodológico, facilitando a identificação da ferramenta correta para o seu trabalho.
4.1. Estudos Observacionais
Esta categoria engloba estudos de coorte, caso-controle e transversais (seccionais). Devido à natureza não experimental, estes estudos são mais suscetíveis a vieses de seleção e confusão, exigindo um relato rigoroso de como essas variáveis foram tratadas.
STROBE (Strengthening the Reporting of Observational Studies in Epidemiology)
- É a diretriz padrão-ouro para relatar estudos observacionais. O checklist do STROBE orienta o autor a descrever com precisão o desenho do estudo, o cenário, os participantes, as variáveis, as fontes de dados e os métodos estatísticos para controle de viés.
- URL: https://www.strobe-statement.org
MOOSE (Meta-analysis of Observational Studies in Epidemiology)
- Enquanto o PRISMA (ver seção 4.3) é usado para revisões gerais, o MOOSE é especificamente desenhado para metanálises de estudos observacionais, abordando desafios únicos como a heterogeneidade entre estudos não randomizados.
- Referência: Stroup DF, et al. JAMA. 2000. (Disponível via Equator Network).
STREGA (Strengthening the Reporting of Genetic Association Studies)
- Uma extensão do STROBE focada especificamente em estudos de associação genética, garantindo que detalhes sobre genotipagem, estrutura populacional e equilíbrio de Hardy-Weinberg sejam reportados.
- URL: https://www.equator-network.org/reporting-guidelines/strobe-strega
Newcastle-Ottawa Scale (NOS)
- Diferente das anteriores (que são guias de relato), a NOS é uma ferramenta de avaliação de qualidade. Ela é amplamente utilizada em revisões sistemáticas para julgar o risco de viés em estudos de coorte e caso-controle primários incluídos na revisão. Existem adaptações também para estudos transversais.
- URL: https://www.ohri.ca/programs/clinical_epidemiology/oxford.asp
4.2. Ensaios Clínicos e Intervenções
Esta é a área com maior rigor metodológico exigido, pois os resultados influenciam diretamente a conduta médica. A transparência sobre como a intervenção foi alocada e como os participantes foram acompanhados é inegociável.
CONSORT (Consolidated Standards of Reporting Trials)
- O padrão global para Ensaios Clínicos Randomizados (ECAs). O checklist foca na descrição detalhada da randomização, cegamento e fluxo de participantes.
- Nota Importante: Conforme as diretrizes atuais, todo ECA deve incluir no manuscrito o número de registro do ensaio (em plataformas como ClinicalTrials.gov ou ReBEC) e o local onde o protocolo completo pode ser acessado.
- URL: https://www.consort-statement.org
SPIRIT (Standard Protocol Items: Recommendations for Interventional Trials)
- Enquanto o CONSORT é usado para relatar os resultados finais, o SPIRIT é utilizado para definir o Protocolo do estudo antes mesmo de ele começar. Revistas exigem cada vez mais a publicação ou disponibilização do protocolo para garantir que os desfechos analisados foram os planejados originalmente, evitando a “pesca de dados” (p-hacking).
- URL: https://www.consort-spirit.org
TREND (Transparent Reporting of Evaluations with Nonrandomized Designs)
- Utilizado para estudos de intervenção que não utilizam randomização (estudos quase-experimentais, saúde pública, comportamentais). Fundamental para explicar como os grupos de comparação foram formados na ausência do sorteio aleatório.
- URL: https://www.cdc.gov/hivpartners/php/trend-statement
REFLECT (Reporting Guidelines for Randomized Controlled Trials for Livestock and Food Safety)
- Uma adaptação do CONSORT voltada especificamente para ensaios clínicos em pecuária e segurança alimentar, reconhecendo as unidades de intervenção que muitas vezes são rebanhos ou grupos, e não indivíduos isolados.
- URL: https://www.equator-network.org/reporting-guidelines/reflect
4.3. Revisões Sistemáticas e Metanálises
As revisões sistemáticas condensam grandes volumes de informação para responder a perguntas clínicas específicas. Dada a sua influência na tomada de decisão, é imperativo que o processo de busca, seleção e análise dos dados seja totalmente transparente para evitar a propagação de erros.
PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses)
- O guia mandatório para relatar revisões sistemáticas e metanálises. O PRISMA exige um fluxograma detalhado (Flow Diagram) que mostre o número de artigos identificados, triados, elegíveis e incluídos, explicando as razões para cada exclusão.
- Nota: Assim como nos ensaios clínicos, revisões sistemáticas devem ter seu protocolo registrado prospectivamente (ex: na plataforma PROSPERO) e es comse número de registro deve constar no artigo final.
- URL: https://www.prisma-statement.org
ROBIS (Risk of Bias in Systematic Reviews)
- Enquanto o PRISMA orienta a escrita, o ROBIS é uma ferramenta para avaliar o risco de viés durante a condução da revisão sistemática. Ele ajuda a identificar se os autores da revisão podem ter introduzido distorções ao selecionar ou analisar os estudos primários.
- URL: https://www.bristol.ac.uk/population-health-sciences/projects/robis
AMSTAR 2 (A Measurement Tool to Assess systematic Reviews)
- Ferramenta crítica para avaliar a qualidade metodológica das revisões sistemáticas (incluindo aquelas que incorporam estudos não randomizados).
- Diferenciação importante: O AMSTAR 2 foca na qualidade geral da condução da revisão, enquanto o ROBIS foca especificamente no risco de viés. Ambas são complementares.
- URL: https://amstar.ca
Prosseguindo com o nosso artigo, finalizamos a seção de “Diretrizes por Tipo de Estudo” abordando os estudos de diagnóstico e outras categorias específicas essenciais.
4.4. Estudos de Acurácia Diagnóstica
Estes estudos avaliam a capacidade de um teste (novo ou existente) em identificar corretamente uma doença ou condição, comparando-o a um padrão de referência (gold standard).
STARD (Standards for Reporting of Diagnostic Accuracy Studies)
- Essencial para garantir que os leitores compreendam o potencial de generalização dos resultados. O checklist exige a descrição detalhada da população, do teste índice, do padrão de referência e de como os resultados indeterminados foram tratados.
- URL: https://www.equator-network.org/reporting-guidelines/stard/
QUADAS-2 (Quality Assessment of Diagnostic Accuracy Studies)
- É a ferramenta padrão para avaliar a qualidade metodológica e o risco de viés em estudos de acurácia diagnóstica, sendo frequentemente utilizada dentro de revisões sistemáticas desta área.
- URL: https://www.bristol.ac.uk/population-health-sciences/projects/quadas/quadas-2/
4.5. Outras Diretrizes Específicas
A pesquisa em saúde é vasta, e existem checklists para desenhos que fogem dos modelos epidemiológicos tradicionais:
CARE (Case Reports)
- Para Relatos de Caso. Embora sejam níveis de evidência mais baixos, relatos de caso são fundamentais para vigilância e educação. O CARE padroniza a descrição de casos clínicos raros ou efeitos adversos, garantindo que informações vitais não sejam perdidas.
- URL: https://www.care-statement.org
ARRIVE (Animal Research: Reporting of In Vivo Experiments)
- Para estudos pré-clínicos envolvendo animais. Visa melhorar a reprodutibilidade da pesquisa básica, exigindo detalhes sobre alojamento, linhagem dos animais e métodos de eutanásia.
- URL: https://arriveguidelines.org/
COREQ (Consolidated Criteria for Reporting Qualitative Research)
- Para pesquisa Qualitativa (entrevistas, grupos focais). Substitui recomendações mais antigas ou dispersas, focando na reflexividade do pesquisador e no contexto do estudo.
- URL: https://www.equator-network.org/reporting-guidelines/coreq/
AGREE II (Appraisal of Guidelines for Research & Evaluation)
- Utilizado não para estudos primários, mas para avaliar a qualidade de Diretrizes Clínicas (Guidelines) já desenvolvidas, verificando o rigor com que as recomendações foram criadas.
- URL: https://www.agreetrust.org/agree-ii/
CHEERS (Consolidated Health Economic Evaluation Reporting Standards)
- Para avaliações Econômicas em saúde (estudos de custo-efetividade, custo-utilidade), cruciais para a gestão em saúde pública.
- URL: https://www.equator-network.org/reporting-guidelines/
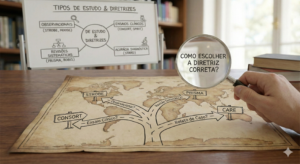
5. Como Escolher a Diretriz Correta?
Com tantas siglas disponíveis, selecionar a ferramenta adequada pode parecer complexo. Abaixo, apresentamos um guia rápido de decisão baseado na pergunta central da sua pesquisa:
- Você está relatando um caso clínico único ou uma série de casos? Use CARE.
- Você realizou uma intervenção (medicamento, cirurgia, fisioterapia)?
- Foi um sorteio aleatório (randomizado)? Use CONSORT.
- Não houve randomização? Use TREND.
- É apenas o protocolo do estudo (ainda não tem resultados)? Use SPIRIT.
- Você está apenas observando pacientes sem intervir (analisando fatores de risco, prognóstico)? Use STROBE (escolha a extensão para coorte, caso-controle ou transversal).
- Você está testando a eficácia de um novo exame diagnóstico? Use STARD.
- Você está resumindo a literatura existente (revisão)?
- É uma revisão sistemática ou metanálise? Use PRISMA.
- É uma metanálise apenas de estudos observacionais? Use MOOSE.
Dica de Ouro: Não deixe para consultar o checklist apenas no momento da submissão. Utilize a diretriz correta durante a escrita do manuscrito. Isso garante que nenhum dado metodológico crítico seja esquecido, evitando retrabalho solicitado pelos revisores.
6. Considerações Finais
A adoção de diretrizes de relato (reporting guidelines) representa um marco de amadurecimento na comunidade científica. Mais do que meras exigências burocráticas, ferramentas como CONSORT, STROBE e PRISMA são instrumentos de transparência que devolvem valor social à pesquisa.
Ao seguir esses checklists, o pesquisador garante que seu trabalho seja:
- Reproduzível: Outros cientistas conseguem entender e replicar seus métodos.
- Utilizável: Os dados podem ser incluídos em futuras metanálises sem risco de viés por falta de informação.
- Confiável: Leitores e revisores conseguem avaliar a validade interna do estudo com clareza.
Em um cenário de produção científica crescente, a qualidade do relato é o diferencial que destaca um estudo relevante da massa de publicações.
Recomendamos que todos os pesquisadores, desde alunos de iniciação científica até líderes de grupos de pesquisa, incorporem a consulta à Rede Equator como passo obrigatório no planejamento e redação de seus trabalhos.
***